Что мы делаем. Каждая страница проходит через несколько сотен совершенствующих техник. Совершенно та же Википедия. Только лучше.
Источник: http://wiki2.org/ru/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Содержание
Открытие
Акролеин был открыт в 19 веке австрийским химиком Йозефом Редтенбахером при сухой перегонке жиров. В ходе своих исследований ученый также открыл и пропенову кислоту.
Источник: http://info-farm.ru/alphabet_index/a/akrolein.html
Это интересно: Военная присяга — освещаем все нюансы
Из Википедии — свободной энциклопедии
 |
|
 |
|
| Систематическое наименование |
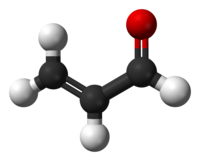
Проп-2-ен-1-аль |
|---|---|
| Традиционные названия | Акролеин, пропеналь, акрилальдегид |
| Хим. формула | C3H4O |
| Молярная масса | 56,0633 ± 0,003 г/моль |
| Плотность | 0,843 г/см³ |
| Энергия ионизации | 974,7911 кДж/моль |
| Т. плав. | −87 °C |
| Т. кип. | 52,7 °C |
| Т. всп. | -26 °C |
| Т. свспл. | 234 °C |
| Пр. взрв. | 2,8–31 % % |
| Кр. точка | 232,85° С |
| Давление пара | 29 кПа (20° С) |
| Растворимость в воде | 200 г/100 мл |
| Дипольный момент | 2,552 ± 0,003 (цис-положение), 3,117 ± 0,004 (транс-положение) |
| Рег. номер CAS | 107-02-8 |
| PubChem | 7847 |
| Рег. номер EINECS | 203-453-4 |
| SMILES |
C=CC=O |
| InChI |
1S/C3H4O/c1-2-3-4/h2-3H,1H2 HGINCPLSRVDWNT-UHFFFAOYSA-N |
| RTECS | AS1050000 |
| ChEBI | 15368 |
| Номер ООН | 1092 |
| ChemSpider | 7559 |
| ПДК | 0,03 мг/м3 |
| ЛД50 | 46 мг/кг (белые крысы, перорально); 7 мг/кг (кролики, перорально); 28 мг/кг (мыши, перорально) |
| Токсичность |
высокотоксичен, особенно опасны его пары, сильный ирритант, лакриматор |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Акролеин (лат. acris — острый, едкий + oleum — масло) (пропеналь) — H2C=CH-CHO, альдегид акриловой кислоты, простейший ненасыщенный альдегид. Бесцветная легколетучая слезоточивая жидкость с резким запахом, сильный лакриматор.
Источник: http://wiki2.org/ru/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Реакционная способность
Акролеин, будучи непредельным альдегидом, проявляет реакционную способность, свойственную как олефинам, так и альдегидам. Так, акролеин образует ацетали:
его альдегидная группа легко окисляется до карбоксильной:
и восстанавливается до гидроксильной:
Карбонильная группа акролеина находится в сопряжении с двойной связью, что обуславливает его высокую реакционную способность по отношению к нуклеофилам, при этом присоединение идёт по β-атому углерода:
Галогены присоединяются к акролеину по двойной связи с образованием дигалогенпроизводного, которое далее отщепляет галогеноводород с образованием α-галогенакролеина:
Благодаря наличию электронакцепторной альдегидной группы, сопряженной с двойной связью, акролеин является диенофилом и реагирует с диенами с образованием продуктов циклоприсоединения (реакция Дильса-Альдера):
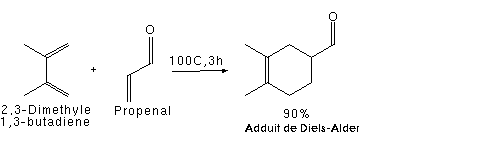
Источник: http://ru.wikipedia.org/wiki/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Синтез
В лаборатории акролеин получается дегидратацией глицерина в присутствии гидросульфата калия.
В промышленности акролеин получают каталитическим окислением пропилена над оксидными висмут-молибденовыми катализаторами или оксидом меди. Ранее в промышленности был распространён процесс парофазной кротоновой конденсации ацетальдегида с формальдегидом (устаревший метод):
Источник: http://wiki2.org/ru/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Химические свойства
Акролеин, благодаря явлению таутомерии, находится в постоянном равновесии со своим изомер — пропадиенолом. Это равновесие может быть смещена действием кислотного или основного катализатора:
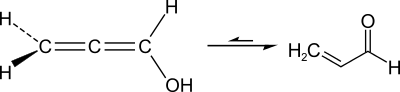
Поскольку акролеин является ненасыщенным альдегидом, то в химических реакциях он проявляет свойства как алкенов, так и альдегидов. В частности акролеин вступает в реакцию гидрогенування, с помощью которой можно получить аллиловый спирт
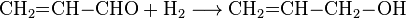
Кроме этого, с помощью действия катализаторов на основе никеля, палладия и платины, реакцию гидрогенування можно повести другим путем и через промежуточное образование пропаналя получить 1-пропанол:
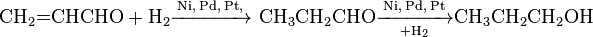
В результате хлорирования акролеина получают α, β-дихлоропропаналь. В промышленности α, β-дихлорпропаналь действием соляной кислоты превращают в α-хлоракролеин, который является сырьем для получения α-хлоракрилатних смол:
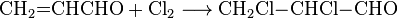
Воздействие на акролеин хлорноватистая кислота приводит к образованию глицеральдегид:
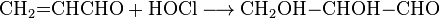
Для акролеина характерна реакция окисления с образованием пропеновои кислоты:
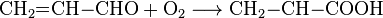
Гидролиз акролеина может проходить двумя путями. В результате образуются 1,3-пропандиол или сложная димерних состав:
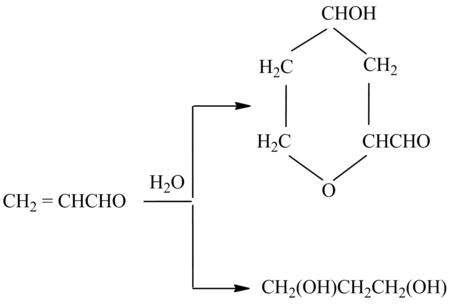
Интересна взаимодействие акролеина с аммиаком, в результате которой происходит циклизация с образованием β-пиколина:
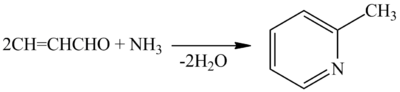
Как и любая ненасыщенная соединение, акролеин способен соединять собственные молекулы. Так в результате димеризации образуются димеры следующей строения:

а полимеризация приводит к образованию полиакролеину.
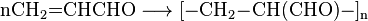
Также с акролеина можно получить незаменимую аминокислоту — метионин. Упрощенно этот процесс записывается следующим образом:
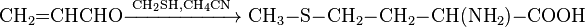
Путем реакции Скраупа ароматических аминов с акролеин, который образуется in situ из глицерина в присутствии дегидратирующего агента и окислителя, получают замещены хинолины:
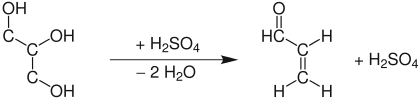
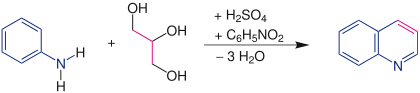
Источник: http://info-farm.ru/alphabet_index/a/akrolein.html
Это интересно: Антропогенное загрязнение
Токсичность
Вследствие своей высокой реакционной способности акролеин является токсичным, сильно раздражающим слизистые оболочки глаз и дыхательных путей соединением, сильный лакриматор. Максимально разовая Предельно допустимая концентрация в воздухе 0,03 мг/м³; Среднесуточная Предельно допустимая концентрация в воздухе 0,01 мг/м³(Список ПДК ГН 2.1.6 1338-03). Вызывает мутагенез у бактерий и дрожжей, проявляет мутагенные свойства на культурах клеток млекопитающих.
Относится к I классу опасности (чрезвычайно опасные вещества).
Акролеин является одним из продуктов термического разложения глицерина и жиров-глицеридов, чем объясняются раздражающие слизистые оболочки свойства дыма горелого жира.
Источник: http://wikipedia.green/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Применение
Наибольшее количество акролеина расходуется на синтез глицерина без использования хлора, где акролеин гидрогенизують к аллилового спирта, затем с помощью перекиси водорода превращают в глицерин.
Наряду с производством аллилового спирта для синтеза глицерина одной из основных областей применения акролеина является синтез метионина. При взаимодействии акролеина с метилмеркаптаном в присутствии катализаторов (пиридин, ацетат меди, пиперидин, этилат натрия) в результате ряда превращений образуется метионин.
Реакция акролеина с многофункциональными соединениями приводит к интересным конденсационных полимеров, среди которых особенно известны Полиацетали с многоосновными спиртами. При полимеризации продукта конденсации с пентаэритрита (торговая марка «ультра-лон») получают вещества с хорошей прочностью на разрыв, высокой ударной прочностью, стойкостью к истиранию. Но эти продукты обладают невысокой теплостойкостью (65-104 ° C).
В результате гидролиза продукта димеризации акролеина и его дальнейшего гидрирования образуется 1,2,6-гексантриол, который применяется как пластификатор и составная часть при производстве алкидных и полиэфирных смол.
Источник: http://info-farm.ru/alphabet_index/a/akrolein.html
Физиологическое воздействие
Общий характер действия
Общий характер действия акролеина выражается в сильном раздражении слизистых оболочек. Кроме этого ненасыщенный альдегид обладает некоторой общей токсичным и слабой наркотической действиями.
Влияние на животных
Острое отравление животных акролеин обычно имеет летальный исход. Так, большинство белых мышей погибает после нескольких минут пребывания в среде с концентрацией акролеина 0,02-0,3 мг / л, а 0,0075 мг / л переносится в течение нескольких часов без серьезных симптомов отравления. Ингаляция паров акролеина вызывает у белых крыс и морских свинок симптомы бронхиальной астмы. Кроме астмы также вызывает эмфизему, полнокровие и расширение капилляров легких, бронхоспазм, поражает нервную систему (прогрессирующие параличи). В результате раздражения слизистых оболочек дыхательных путей возникает значительный отек гортани, отек и деструкция слизистой и подслизистой трахеи и крупных бронхов вплоть до закрытия их просвета. Концентрации 1 и 0,75 мг / л вызывают гибель крыс. При 0,65 мг / л гибель происходит чаще осложнений — возникновение вторичной инфекции и пневмонии. У кошек при 0,25 мг / л возникает слюнотечение, слезотечение, легкий наркоз; при 0,2 мг / л — сильное раздражение легких; при 1,5 мг / л и воздействии 2,5 ч, а также при 2 мг / л и влиянии 2 часа — гибель. Вскрытие показывает, что гибель происходит вследствие ожогов слизистой оболочки верхних дыхательных путей и кровоизлияний и отеков в легких.
Хроническое отравление, возникающее при длительном воздействии акролеина на организм животного приводит к тяжелым последствиям для здоровья. При вдыхании акролеина с концентрацией 0,6 мг / л в течение 6 месяцев наблюдались точечные кровоизлияния на слизистой оболочке дыхательных путей, деструкция бронхов с частичным закрытием их просвета. Введение акролеина через рот в течение такого же срока 0,5 мг / кг вызвало нарушение функции почек, а на вскрытии обнаруживали воспалительные изменения в легких и дистрофические изменения в печени и миокарде.
Воздействие на человека
При кратковременном вдыхании небольших концентраций акролеина человеком возникает жжение в глазах, слезотечение, конъюнктивит, отек век, ощущение жжения в горле, кашель и т. Д .. При больших концентрациях возникают резкие явления раздражения, кроме того, легкое головокружение, приливы крови к головы, боли в животе, тошнота, рвота, посинение губ, акроцианоз. В тяжелых случаях — замедление пульса, гипогликемия, слюнотечение, снижение температуры конечностей, онемение кончиков пальцев, расширение зрачков, приглушенные тоны сердца и даже потеря сознания. Отмечались также состояние возбуждения, дезориентация в пространстве и времени. В легких случаях выздоровление длилось 1-2 дня, в более тяжелых случаях — 4-5 дней. Известно смертельное отравление одного из двух рабочих, которые осуществляли в течение двух часов автогенная сварки внутри котла, служивший для транспортировки рапсового масла.
Пребывание человека в среде с концентрацией акролеина 0,35 мг / л в течение 10 мин является смертельным; вдыхание воздуха с содержанием 0,002 мг / л акролеина в течение 2-3 мин вызывает раздражение глаз и носа; через 5 мин раздражение становится невыносимым; концентрация 0,0006 мг / л вызывает умеренное раздражение при вдыхании в течение 5 минут. Порог восприятия запаха 0,00007 мг / л. Пороговая концентрация по рефлекторным действием 0,00005 мг / л.
При хронических отравлениях человеческого организма акролеин может развиваться повышенная чувствительность к соединения.
Источник: http://info-farm.ru/alphabet_index/a/akrolein.html
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.
Источник: http://wiki2.red/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD
Количество использованных доноров: 5
Информация по каждому донору:
- http://ru.wikipedia.org/wiki/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD: использовано 1 блоков из 7, кол-во символов 858 (8%)
- http://wiki2.org/ru/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD: использовано 3 блоков из 8, кол-во символов 2083 (20%)
- http://wikipedia.green/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD: использовано 1 блоков из 7, кол-во символов 701 (7%)
- http://info-farm.ru/alphabet_index/a/akrolein.html: использовано 4 блоков из 6, кол-во символов 6750 (64%)
- http://wiki2.red/%D0%90%D0%BA%D1%80%D0%BE%D0%BB%D0%B5%D0%B8%D0%BD: использовано 1 блоков из 8, кол-во символов 128 (1%)










