 |
|
 |
|
| Систематическое наименование |
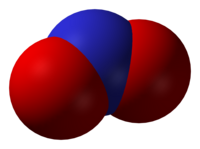
Оксид азота(IV) |
|---|---|
| Хим. формула | NO2 |
| Состояние | бурый газ или желтоватая жидкость |
| Молярная масса | 46,0055 г/моль |
| Плотность | г. 2,0527 г/л ж. 1,4910г/см³ тв. 1,536 г/см³ |
| Энергия ионизации | 1,6E-18 Дж |
| Т. плав. | -11,2 °C |
| Т. кип. | +21,1 °C |
| Энтальпия образования | 33,10 кДж/моль |
| Давление пара | 720 ± 1 мм рт.ст. |
| Рег. номер CAS | 10102-44-0 |
| PubChem | 3032552 |
| Рег. номер EINECS | 233-272-6 |
| SMILES |
N(=O) |
| InChI |
1S/NO2/c2-1-3 JCXJVPUVTGWSNB-UHFFFAOYSA-N |
| RTECS | QW9800000 |
| ChEBI | 33101 |
| Номер ООН | 1067 |
| ChemSpider | 2297499 |
| NFPA 704 | 
ОХ |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Оксид азота (IV) (диоксид азота) NO2 — ядовитый газ, красно-бурого цвета, с резким неприятным запахом, или желтоватая жидкость.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона.
При температуре 140 °C диоксид азота состоит только из молекул NO2, но очень тёмного, почти чёрного цвета.
В точке кипения NO2 представляет собой желтоватую жидкость, содержащую около 0,1 % NO2.
При температуре ниже +21°С — это бесцветная жидкость (или желтоватая из-за примеси мономера).
При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Источник: http://wiki2.org/ru/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B0%D0%B7%D0%BE%D1%82%D0%B0(IV)
Содержание
Получение
В лаборатории NO2 обычно получают воздействием концентрированной азотной кислоты на медь:
.
Также взаимодействием нитритов с серной кислотой:
,
оксид азота(II) NO тотчас же реагирует с кислородом:
/
Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность:
Разработан более совершенный лабораторный способ получения NO2.
Последняя реакция была разработана и реализована в новой химической машине — генераторе окислителя ракетного топлива марки NTO согласно ГОСТ Р ИСО 15859-5-2010.
Другие способы получения оксида азота(IV) перечислены в статье .
Источник: http://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B0%D0%B7%D0%BE%D1%82%D0%B0(IV)
Краткая характеристика оксида азота (IV):
Оксид азота (IV) – неорганическое вещество, ядовитый газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость.
Оксид азота (IV) содержит один атом азота и два атома кислорода.
Химическая формула оксида азота (IV) NO2.
В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона.
При температуре 140 °C оксид азота (IV) состоит только из молекул NO2, но очень тёмного, почти чёрного цвета.
В точке кипения NO2 – +21,1 °C представляет собой желтоватую жидкость, содержащую около 0,1 % NO2.
При температуре ниже +21°С – это бесцветная жидкость (или желтоватая из-за примеси мономера).
При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4.
Кислотный оксид.
Оксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
Источник: http://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/oksid-azota-iv-dioksid-azota-svoystva-poluchenie-himicheskie-reaktsii/
Химические свойства
Кислотный оксид. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
Жидкий NO2 применяется для получения безводных нитратов:
В реакциях с галогенами образует соли нитрония, нитрозила и оксиды галогенов:
Источник: http://wiki2.org/ru/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B0%D0%B7%D0%BE%D1%82%D0%B0(IV)
Применение и использование оксида азота (IV):
Оксид азота (IV) используется при производстве серной и азотной кислот, а также в качестве окислителя в жидком ракетном топливе.




карта сайта
оксид азота (IV) реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида азота (IV)
реакции с оксидом азота (IV)
comments powered by HyperComments
Источник: http://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/oksid-azota-iv-dioksid-azota-svoystva-poluchenie-himicheskie-reaktsii/
Количество использованных доноров: 3
Информация по каждому донору:
- http://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B0%D0%B7%D0%BE%D1%82%D0%B0(IV): использовано 1 блоков из 9, кол-во символов 630 (15%)
- http://wiki2.org/ru/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B0%D0%B7%D0%BE%D1%82%D0%B0(IV): использовано 2 блоков из 9, кол-во символов 2153 (50%)
- http://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/oksid-azota-iv-dioksid-azota-svoystva-poluchenie-himicheskie-reaktsii/: использовано 2 блоков из 7, кол-во символов 1561 (36%)






